ТИАЗОЛ
(1,3-тиазол),
мол. м. 85,13; бесцв. жидкость с запахом пиридина; раств. в орг. р-рителях и
в воде; т. кип. 117-118 °С;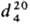 1,198;
1,198;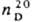 1,5969.
Основание (рКа 2,53); для 4-метилтиазола рКа
3,07. Т., как и др. азолы
,-6 p-электронная гетероароматич. система.
По хим. св-вам близок к пиридину
и тиофену
.
1,5969.
Основание (рКа 2,53); для 4-метилтиазола рКа
3,07. Т., как и др. азолы
,-6 p-электронная гетероароматич. система.
По хим. св-вам близок к пиридину
и тиофену
.
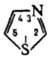
Производные Т. обычно
с трудом вступают в р-ции электроф. замещения, что обусловлено N-протонированием
или комплексообразованием с к-тами Льюиса в условиях р-ции. В условиях, исключающих
эти р-ции, бромирование Вr2 в бензоле и нитрование в уксусном ангидриде
или тетрафтороборатом N-нитропиколиния в ацетонитриле идут в положение 5. Реакц.
способность разл. положений тиазольного цикла при электроф. замещении, протекающем
через катионный s-комплекс, уменьшается в ряду: 5->4-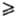 2-положение.
Важную роль в химии Т. играют р-ции электроф. замещения, идущие по т. наз. илидному
механизму, напр. р-ция изотопного обмена:
2-положение.
Важную роль в химии Т. играют р-ции электроф. замещения, идущие по т. наз. илидному
механизму, напр. р-ция изотопного обмена:
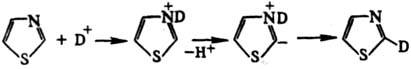
В р-циях нуклеоф. замещения
наиб. активно положение 2, по к-рому протекают прямое нуклеоф. замещение атома
H на аминогруппу по Чичибабина реакции
и металлирование.
Под действием окислителей
(напр., надкислот) Т. и его замещенные окисляются в соответствующие N-оксиды,
способные к 1,3-диполярному присоединению. Т. и его производные устойчивы к
действию водорода в момент выделения, а также в присут. катализаторов, однако
под действием NaBH4 превращ. в тетрагидротиазолы (тиазолидины). При
действии Ni-Ренея претерпевают десульфуризацию с образованием алифатич. соединений.
Важное синтетич. значение
имеет подвижность атома водорода метилъной группы в положении 2 тиазолиевых
солей, к-рая используется в синтезе цианиновых красителей, напр. по р-ции:
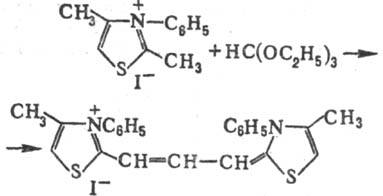
Осн. методы синтеза Т.
и его замещенных: взаимод. a-галогенкетонов или a-галогенальдегидов
с тиоамидами (см. Ганча синтезы
), циклизация a-тиоцианокетонов
под действием водных р-ров к-т или безводного НСl либо РОСl3, взаимод.
ациламинокарбонильных соед. с P2S5, напр.:
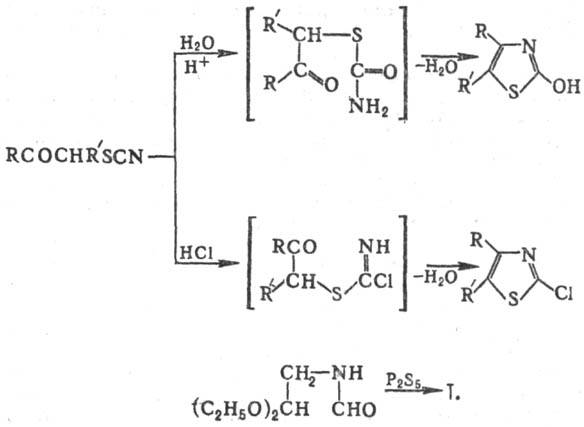
Важнейшее прир. соед. ряда
Т.-тиамин (витамин В1), молекула к-рого включает фрагмент соли тиазолия.
Мн. производные Т.-лек. препараты, напр. норсульфазол - 2-сульфаниламидотиазол
и фталазол [2-(N-о-карбоксибензо-илсульфанил)амидотиазол]. Тиазолидиновое
кольцо-структурный фрагмент пенициллина и разнообразных полу-синтетич. пенициллинов.
Нек-рые производные Т.-красители, используемые в т. ч. и в цветной фотографии.
Лит.: Гетероциклические
соединения, под ред. Р. Эльдерфильда, пер. с англ., т. 5, М., 1961, с. 395-584;
Thiazole and its derivatives, ed. by J. V. Metzger, pt 1-3, N. Y., 1979; Comprehensive
heterocyclic chemistry, ed. by A. R. Katritzky, C. W. Rees, v. 4, Oxf., 1984.
Л.И. Беленький.
|

